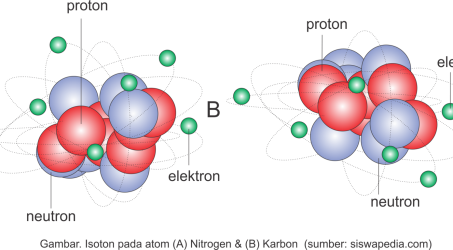
Partikel Penyusun Atom – Istilah Atom pertama kali diperkenalkan ke publik oleh Democritus yang diambil dari kata atomos dimana yang dalam bahasa Yunani a berarti tidak dan tomos berarti dibagi. Dengan kata lain atom merupakan partikel terkecil yang tidak bisa dibagi lagi. Diameternya bisa sekitar 3 hingga 5 nm.
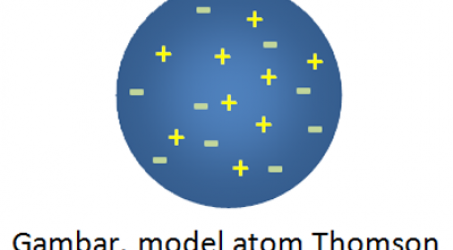
Hingga hari ini belum ada teknologi yang bisa memberi gambaran asli dari wujud atom secara jelas. Para ilmuwan hanya bisa memprediksi kemudian membuat model atom berdasarkan sifat-sifatnya. Penelitian atom terus berkembang, berbagai perubahan model atom pernah dikemukakan oleh para ahli. Misalnya saja teori atom Dalton, Thomson, Rutherford dan Bohr. Kita akan membahasnya di halaman lain yang berjudul Perkembangan Teori Atom.
Apa sajakah partikel penyusun atom itu ?
Penggaris plastik merupakan materi yang tersusun dari atom. Apa itu materi? Silahkan baca artikel berjudul Materi dan Wujudnya. Penggaris ini bila kita gosokkan ke rambut yang kering, maka akan dapat menarik sobekan-sobekan atau potongan kertas berukuran kecil. Darisini kita akan mengetahui bahwa penggaris plastik memiliki sifat listrik. Oleh karena penggaris plastic terdiri dari atom, maka bisa dikatakan bahwa atom memiliki sifat listrik.
Sifat kelistrikan pada atom diteliti oleh para ilmuwan diantaranya J.J. Thompson, Eugen Goldstein, Ernest Rutherford, W. Bathe, H. Becker dan James Chadwick.
A. Proton
Eugen Goldstein pada tahun 1886 melakukan percobaan dengan memodifikasi tabung sinar katode yang ditemukan oleh William Crookes dengan cara melobangi lempeng katode. Dari percobaan ini ditemukan bahwa gas yang berada di belakang katode menjadi berpijar. Hal ini berarti radiasi dari anode menembus lempengan katode melalui lubang yang sebelumnya telah dibuat.
-
- Sifat sinar anode ini yaitu:
Merupakan radiasi partikel karena mampu memutar baling-baling. - Radiasi ini bila dibelokkan menggunakan medan magnet, maka akan menuju ke kutub magnet negatif. Itu artinya radiasi sinar ini bermuatan positif (itulah sebabkan kemudian dinamakan anode yang kemudian dinamakan proton).
- Partikel sinar anode bergantung pada jenis gas yang ada di dalam tabung.
- Sifat sinar anode ini yaitu:
Massa proton terkecil diperoleh pada atom Hidrogen yaitu Massa 1 proton = 1 sma = 1,66 × 10-24 gram dengan muatan 1 proton = +1 = 1,6 × 10-19 C.
B. Elektron
Joseph John Thomson pada tahun 1897 melakukan percobaan dengan menggunakan tabung sinar katode. Terdapat dua plat elektroda dimana salah satu plat logam yang terdapat pada ujung tabung berfungsi sebagai katoda. Kedua plat ini dimasukkan ke dalam tabung kaca bertekanan rendah kemudian dialirkan listrik bertegangan tinggi hingga mampu melepas elektron dari katoda ke anoda.
Sinar katoda tidak dapat kita lihat menggunakan mata telanjang namun kita bisa mengetahui bahwa sinar ini ada dari berpenjarnya lapisan tabung kaca bagian dalam akibat adanya benturan antara elektron dengan dinding tabung. Atau kita bisa melihatnya jika sinar katoda kita benturkan ke layar ber-fluoresensi (layar yang dapat berpendar) setelah terlebih dahulu kita beri lubang pada plat logam anoda. Seperti gambar di bawah ini.
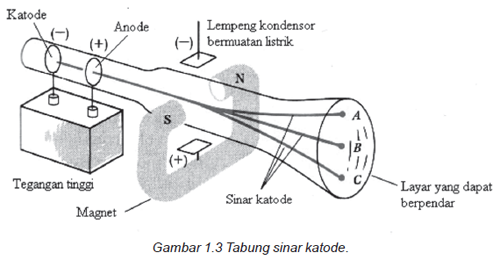
Dari hasil percobaannya ditemukan sifat sinar katode yaitu:
-
- Merupakan radiasi partikel karena mampu memutar baling-baling.
- Radiasi ini bila dibelokkan menggunakan medan magnet, maka akan menuju ke kutub magnet positif. Itu artinya sinar katode bermuatan negatif.
- Partikel katoda merambat tegak lurus dari lempengan katode menuju anode.
- Sinar katoda tidak tergantung pada jenis plat logam yang digunakan.
- Sinar katoda dapat kita buat dengan listrik tegangan tinggi.
Dari sifat inilah kemudian oleh J.J Thomson menamakan partikel penyusun atom bermuatan negatif ini sebagai elektron. Setelain ini J.J Thomson juga menemukan perbandingan muatan elektron terhadap massa yaitu 1,76 × 108 C/g yang kemudian pada tahun 1909, Robert Millikan berhasil menemukan besarnya muatan sebuah elektron yaitu 1,6 × 10-19 C. Dengan demikian, maka kita peroleh massa 1 elektron sebesar 9,1095×10-31 Kg.
C. Neutron
Setelah ditemukan adanya proton di dalam inti atom, didapati bahwa ternyata massa inti atom selalu lebih besar daripada proton. Darisinilah kemudian para peneliti berpendapat bahwa ada partikel lain di dalam inti (selain proton) yang muatannya netral.
W. Bothe dan H. Becker pada tahun 1930 melakukan penembakan menggunakan partikel alpha (α) ke inti atom berilium. Ditemukan adanya radiasi partikel yang memiliki daya tembus besar. Dua tahun sesudahnya yaitu tahun 1932, James Chadwick melakukan penelitian lebih lanjut dimana ditemukan bahwa partikel tersebut bermuatan netral dan memiliki massa hampir sama dengan partikel proton (bermuatan positif). Partikel ini kemudian dinamakan sebagai neutron.
Daftar Pustaka
Brown, Theodore L & Lemay, H. Eugene, J.R. 1977. Chemisty, The Central Science.
Prentice-Hall. Inc.
Harnanto, Arie dan Ruminten. 2009. Kimia I. Jakarta: Pusat Perbukuan Departemen Pendidikan Nasional.
Permana, Irvan. 2009. Memahami Kimia I. Jakarta: Pusat Perbukuan Departemen Pendidikan Nasional.
Ratna dkk. 2008. Kimia Jilid 1. Jakarta: Direktorat Pembinaan Sekolah Menengah Kejuruan.