Cara Menentukan Elektron Valensi - Selanjutnya pembahasan kita kali ini adalah tentang teori atom, pada pembahasan ini yang menjadi titik poin pembahasannya yaitu membuat konfigurasi elektron untuk menentukan nilai elektron valensi nya.
Menurut model atom mekanika kuantum, elektron-elektron berada dalam orbital-orbital tertentu yang mengelilingi inti aton yang membentuk kulit atom.
Susunan kulit-kulit atom ini mirip dengan model atomyang dikemukakanoleh Niels Bohr atau biasa dikenal dengan model atom Niels Bohr.
Berikut hasil pengamatan yang dilakukan oleh Niels Bohr pada spektrum atom hidrogen, model atom yang dikelurkan oleh Niels Bohr adalah hasil perbaikan dari model atom Rutherford, dengan menyusun model atom sebagai berikut :
- Atom terdiri atas inti atom yang mengandung proton yang bermuatan positif dan elektron bermuatan negatif yang mengelilinhi inti atom.
- Elektron-elektron yang mengelilingi inti atom berada pada tingkat energi tertentu yang bergerak secara tetap (stasioner).
- Tingkat energi atau lintasan elektron yang paling dekat dengan inti atom mempunyai tingkat energi terrendah, lintasan elektron yang paling jauh dari inti atom memiliki tingkat energi yang lebih tinggi.
- Elektron dapat berpindah dari lintasan yang satu ke lintasan yang lain dengan menyerap atau melepaskan energi unruk menjaga kestabilannya.
Berdasarkan percobaan pada spektrum hidrogen inilah yang berhasil memberikan gambaran keadaan elektron dalam menempati daerah sekitar inti atom.
Menurut model atom Bohr, elektron-elektron mengelilingi inti atom pada lintasan-lintasa tertentu yang disebut kulit atom atau tingkat energi. Kulit yang ditempati elektron bergantung pada energinya.
Tingkat energi yang paling rendah ialah kulit atom yang terletak paling dalam atau paling dekat dengan inti, makin keluar semakin besar nomor kulitnya dan makin besar pula tingkat energinya.
Konfigurasi elektron
Nah sekarang kita akan membahas tentang konfigurasi elektron. Konfigurasi elektron dalam teori atom Bohr dikenal dengan susunan elektron pada masing-masing kulit.
Data yang digunakan untuk menuliskan konfigurasi elektron adalah nomor atom suatu unsur dimana nomor atom tersebut dapat menyatakan jumlah elektron yang terdapat dalam atom tersebut.
Konfigurasi elektron pada dasarnya menggambarkan adanya penyebaran atau susunan elektron dalam atom. Pengisian elektron pada kulit-kulit atom tersebut harus memenuhi aturan-aturan sebagai berikut :
- Jumlah maksimum elektron pada suatu kulit harus memenuhi rumus 2n2. dengan n = nomor kulit.
Kulit K ( n = 1) dengan rumus 2n2maksimum 2. 12 = 2 elektron
Kulit L ( n = 2) dengan rumus 2n2maksimum 2. 22 = 8 elektron
Kulit M ( n = 3) dengan rumus 2n2maksimum 2. 32 = 18 elektron
Kulit N ( n = 4) dengan rumus 2n2maksimum 2. 42 = 32elektron, dan seterusnya.
- Lambang kulit dimulai dari K, L, M, N, dan seterusnya sesuai susunan abjad dimulai dari yang terdekat dengan inti atom.
Elektron disusun sedemikian rupa pada masing-masing kulit dan diisi maksimum sesuai daya tempung kulit tersebut. Jika masih ada sisa elektron yang tidak dapat ditampung pada kulit tersebut maka elektronnya akan diletakkan pada kulit selanjutnya
Contoh konfigurasi elekron :
12Na = 2 8 1
20Ca = 2 8 8 2
35Br = 2 8 18 7
Elektron yang terdapat di kulit terluar suatu atom disebut sebagai elektron valensi. Jadi, elekron valensi untuk atom Na adalah 1, elekron valensi dari atom Ca adalah 2, dan elektron valensi sari atom Br adalah 7. Untuk lebih jelas lagi perhatikan konfigurasi elektron pada unsur K dengan nomor atom 19.
Hal ini dapat dijelaskan bahwa elektron paling luar maksimum 8, sehingga sisanya harus 1 berada di kulit terluar. Begitu pula dengan nomor atom 20 dan seterusnya.
Tabel 1.1 Contoh konfigurasi elektron unsur-unsur dari nomor atom 1 samapi 20
Baca juga: Materi dan wujudnya
Prinsip Aufbau
Elektron-elektron dalam suatu atom akan menempati orbital yang memiliki energi yang paling rendah lalu kemudian diteruskan untuk menempati orbital dengan tingkat energi yang lebih tinggi dinamakan Prinsip aufbau. Dengan demikian, atom berada pada tingkat energi paling minimum.
Urutan tingkat energi ditunjukkan pada gambar 1.2.
Untuk pengisian orbital dimulai dari orbital 1s, 2s, 2p, dan seterusnya. Seperti yang terlihat pada gambar bahwa subkulit 3d mempunyai energi lebih tinggi daripada subkulit 4s. Oleh karena itu, setelah 3p terisis penuh maka elektron berikutnya akan mengisi subkulit 4s. Lalu kemudian akan mengisi subkulit 3d.
Contoh soal konfigurasi elektron
Tentukan konfigurasi elekron unsur-unsur berikut berdasarkan prinsip Aufbau:
20Ca
15P
13Al
Jawaban:
20Ca = 1s2 2s2 2p6 3s2 3p6 4s2
15P = 1s2 2s2 2p6 3s2 3p3
13Al = 1s2 2s2 2p6 3s2 3p1
Kaidah Hund
Kaidah Hund adalah distribusi elektron-elektron pada orbital-orbital yang setingkat (energinya sama) dalam suatu orbital satu per satu dengan arah spin yang sma sebelum berpasangan, konfigurasi elektron dapat dituliskan dalam bentuk diagram orbital.
Sepasang elektron yang menghuni suatu Orbital dapat dilambangkan dengan bentuk strip, sedanglan dua elektron penghuni orbital dilambangkan dengan dua anak panah yang saling berlawanan arah ke atas dan ke bawah. Jika orbital hanya mengandung satu elektron, maka anak panah dituliskan mengarah ke atas.
Friedrich Hund (1894-1968) pada tahun 1930 menyatakan bahwa elektron-elektron dalam orbital-orbital suatu sub kulit cenderung tidak berpasangan. Elektron baru akan berpasangan apabila pada subkulit itu sudah tidak ada lagi orbital kosong.
Contoh soal:
Tentukan diagram orbital untuk unsur-unsur berikut:
4Be
8O
Jawab :
4Be = 1s2 2s2 diagram orbitalnya
8O = 1s2 2s2 2p4 diagram orbitalnya
Larangan Pauli
Wolfgang Pauli ( 1900-1958) mengatakan bahwa tidak ada sepasang elektron yang terdapat dalam satu atom yang memiliki keempat bilangan kuantum yang bersamaan, sepasang elektron yang mempunyai keempat bilangan kuantum yang sama dalam satu orbital tersebut harus mempunya spin yang berbeda. Maka kedua elektron tersebut dapat dinyatakan berpasangan.
Pada setiap orbital hanya mampu menampung maksimal dua elektron saja. Untuk mengimbangi gaya tolak menolak di antara elektron-elektron tersebut, dua elektron dalam satu orbital selalu berlawanan arah. Aturan maksimum pengisian elektron dalam setiap subkulit sebagai berikut:
Tabel 1.2 Aturan Pengisian Elektron Pada Subkulit.
Orbital-orbital yang terdapat dalam suatu subkulit mempunyai tingkat energi yang sama, sedangkan orbital-orbital dari subkulitnya itu berbeda, tetapi dari kulit yang sama mempunyai tingkat energi yang mirip.
Cara Menentukan Elektron valensi
Elekton valensi adalah elektron yang berada pada kulit terluar. Elektron yang berada di kulit terluar tersebut dapat berpartisipasi dalam pembentukan ikatan kimia jika masih ada salah satu kulit luarnya yang belum terisi secara penuh.
Sifat-sifat kimia suatu atom dapat diketahui melalui elektron valensinya dan berperan penting dalam pembentukan ikatan dengan atom lain. Elektron valensi atau elektron pada kulit terluar sangat berperan penting dalam reaksi pembentukan ikatan kimia dan reaksi-reaksi kimia antar atom.
Jumlah elektron valensi dalam suatu unsur di tentukan berdasrkan elektron yang terdapat pada kulit terluar dari konfigurasi elektron atom tersebut.
Perhatikan tabel 1.3 untuk cara menentukan jumlah elektron valensi
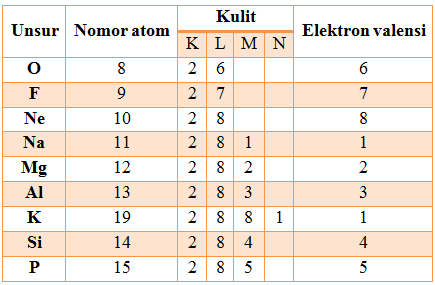
Perlu kalian ketahui bahwa unsur-unsur yang mempunyai jumlah elektron yang sama akan memiliki sifat kimia yang sama pula. Salah satu contohnya adalah unsur kalium dan natrium, kedua unsur ini memiliki sifat kimia yang sama karena masing-masing memiliki elektron valensi yang berjumlah = 1.
Semoga artikel di atas dapat membantu teman-teman dalam memahami dan mengetahui bagaimana cara agar mengetahui elektron valensi suatu atom dengan konfigurasi elekton dan asas-asas yang berlaku dalam konfigurasi elektron.
Baca juga: Perkembangan teori atom
Demikian pembehasan kita kali tentang Cara Menentukan Elektron Valensi ini, jika ada yang kurang dimengerti bisa komentar di kolom komentar yaa, terimakasih.
Referensi:
Pernama Irvan. (2009). Memahai Kimia SMA/MA Untuk Kelas X Semester 1 Dan 2. Pusat Perbukuan Departemen Pendidikan Nasional. Jakarta.
Setyawati A A. (2009). Kimia Mengkaji Fenomena Alam Untuk Kelas X SMA/MA. Pusat Perbukuan Departemen Pendidikan Nasional. Jakarta.
Utami Budi, dkk. (2009). KimiaUntuk SMA/MA Kelas X1 Program Ilmu Alam: Pusat Perbukuan Departemen Pendidikan Nasional. Jakarta.