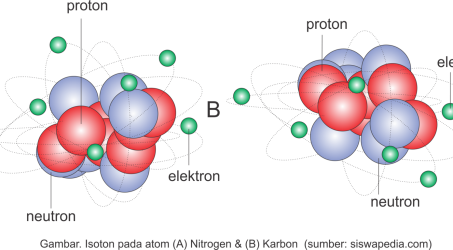
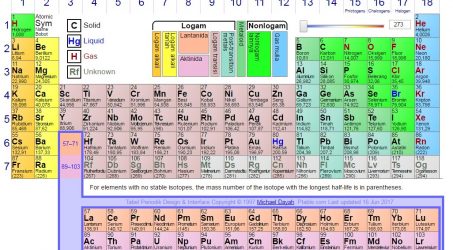
Bagaimana sejarah perkembangan sistem periodik unsur ?
Perkembangan sistem periodik unsur dimulai dari generasi ke generasi secara bertahap (bukan langsung jadi) hingga disusun menjadi seperti saat ini. Susunan yang ada saat inipun bisa saja mengalami perubahan seiring ditemukannya fakta terbaru terkait unsur-unsur.
Perhatikanlah perkembangan sistem periodik unsur secara umum di bawah ini
1. Kimiawan Arab dan Persia: Mengelompokkan unsur dalam dua kelompok yaitu kelompok unsur logam dan non logam.
2. A. Lavoisier: Melakukan pengelompokkan zat berdasarkan sifat kimia.
3. Jhon Dalton: Melakukan pengelompokkan unsur berdasarkan kenaikan massa atom.
4. J.J Berzellius: Membuat daftar massa atom unsur-unsur yang akurat.
5. Triade oleh Dobereiner: Tiap kelompok terdiri dari tiga unsur dimana memiliki sifat yang mirip.
6. Oktaf oleh Newlands: Menyusun periodisasi sifat unsur-unsur berdasarkan nomor massa.
7. Lothar Meyer dan Mendeleyev: Menyusun sistem periodik untuk pertama kalinya berdasarkan kenaikan massa atom dan kemiripan sifat-sifat unsur.
8. Moseley: Berpendapat bahwa urutan kenaikan nomor atom sama dengan urutan kenaikan nomor massa.
9. Sistem periodik modern terus berkembang hingga saat ini.
Baca juga: Memahami unsur dalam ilmu kimia
Mengapa unsur-unsur harus dikelompokkan?
Pada mulanya para ilmuwan melakukan penelitian terkait unsur secara terpisah. Akan tetapi karena jumlah unsur ternyata sangat banyak, maka agar mudah untuk mempelajarinya dibuatlah pengelompokan unsur-unsur.
Seperti pada gambaran di atas, pada mulanya unsur dikelompokan oleh ilmuwan Arab dan Persia berdasarkan sifat logam dan non logam.
Sifat fisika logam antara lain mengkilap, pada suhu kamar pada umumnya akan berbentuk padat, mudah dibentuk atau ditempa serta menjadi penghantar listrik dan panas secara baik.
Sedangkan sifat fisika nonlogam antara lain tidak mengkilap, pada suhu kamar dapat berbentuk cair, padat dan gas, sulit dibentuk serta bukan merupakan penghantar yang baik bagi panas dan listrik.
Kemudian pada perkembangannya, Lavoisier melakukan pengelompokan berdasarkan sifat-sifat kimia zat sehingga unsur dibagi menjadi empat golongan yaitu unsur gas, unsur logam, unsur nonlogam dan unsur tanah.
Ada perkembangan yang pesat setelah Jhon Dalton mengemukkan teorinya bahwa unsur tersusun dari atom yang memiliki sifat dan massa atom berbeda-beda. Sehingga pengelompokan unsur-unsur dilakukan berdasarkan kenaikan massanya.
Pada saat itu peralatan tak cukup canggih untuk bisa menghitung massa sebuah atom tunggal karena massanya sangat kecil. Sehingga para ilmuwan menentukan perbedaan massa atom relatif berdasarkan perbandingan massa atom yang satu dengan yang lainnya. Digunakanlah perbandingannya menggunakan massa atom Hidrogen.
Pada tahun 1814, J.J Berzellius kemudian dilanjutkan pada tahun 1819 oleh P. Dulong dan A. Petit melakukan penelitian penentuan massa atom yang lebih akurat berdasarkan kalor jenis unsur.
Penemuan alat spektrometer massa yakni pada abad 20 membuat penyusunan massa relatif menjadi lebih akurat dimana sebelumnya menggunakan perbandingan terhadap massa atom Hidrogen berubah menjadi menggunakan isotop C-12. Satuannya pun berubah dari gram menjadi sma (Satuan Massa Atom).
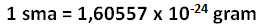
Disini J.J Berzellius melakukan perubahan yang sangat besar yaitu sebuah penentuan massa atom yang lebih akurat.
Pembahasan terkait perkembangan sistem periodik unsur oleh Triade Dobereiner, Oktaf Newlands, Mendeleyev dan sistem periodik modern akan kita bahas pada pembahasan halaman berikutnya.