Macam-Macam Gaya Antar Molekul Beserta Contohnya - Di dalam materi ikatan kimia kita sudah mempelajari bahwa suatu senyawa terbentuk karena atom-atom saling berikatan. Ikatan ini disebabkan karena adanya gaya tarik-menarik antar atom di dalam molekulnya. Apabila gaya ini diganggu atau diberi suatu aktivitas maka akan terjadi reaksi kimia.
Oleh karena itu, dalam pembahasan kali ini akan dipaparkan mengenai gaya antar-molekul. Gaya antar molekul adalah gaya tarik menarik antar molekul-molekul yang jaraknya berdekatan.
Baca juga: Macam-Macam Ikatan Kimia
Secara teori, gaya antar molekul memiliki gaya tarik yang lebih lemah dibandingkan dengan gaya intra molekul (gaya di dalam molekul). Selain itu gaya antar molekul mempengaruhi kepolaran masing-masing molekul dan sifat fisisnya seperti titik beku, titik didih dan titik leleh.
Macam-Macam Gaya Antar Molekul Beserta Contohnya
Ada berapa jenis gaya antar molekul? Berikut ini beberapa jenis gaya antar molekul yang harus anda pelajari.
1. Gaya London (Dispersi)
Apabila suatu elektron bergerak di dalam molekul maupun atom, gerakan tersebut acak sehingga menyebabkan elektron hanya berada di satu sisi molekul atau atom tersebut. Keadaan tersebut membuat partikel menjadi dipol yang hanya berlangsung sesaat sehingga disebut dengan dipol sesaat.
Apabila di salah satu sisi partikel terbentuk sisi negatif, maka sisi yang lainnya akan tertolak. Dengan kata lain, dipol sesaat mampu mempengaruhi dipol di dekatnya. Jika ada dua partikel yang memiliki dipol berbeda berdekatan maka akan terjadi tarikan sementara sehingga kedua partikel menyatu.
Pada atom bebas dan molekul yang bersifat nonpolar, gaya tarikan ini sangat lemah, yang disebut dengan gaya London. Gaya London terjadi di semua partikel. Namun, untuk senyawa ion, pengaruhnya bisa dibilang sangat kecil jika dibandingkan dengan gaya tarik menarik yang terjadi antar ion.
2. Gaya Van der Waals
Gaya antar molekul selanjutnya adalah gaya Van der Waals. Nama gaya ini diambil dari nama seorang ilmuwan yaitu Johannes Van der Waals. Gaya ini terjadi pada molekul-molekul yang terjadi dipol permanen misalnya pada molekul ionik dan kovalen polar. Apabila molekul memiliki kutub yang sama maka keduanya akan tolak menolak. Sebaliknya, jika kutub keduanya berbeda maka akan tarik menarik.
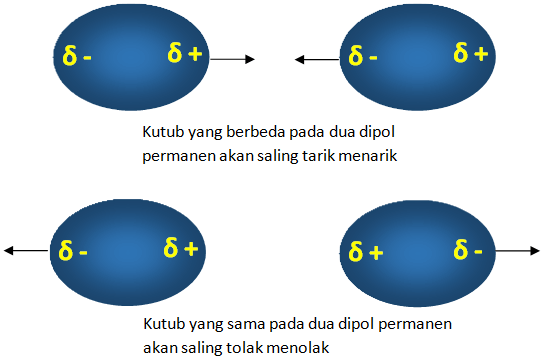
Gaya Van der Waals ini bila terjadi ini apabila terjadi pada molekul polar atau molekul-molekul dipol permanen, maka dinamakan sebagai gaya dipol-dipol. Nah, semakin besar nilai momen dipol yang dimiliki molekul-molekulnya, maka akan semakin besar gayanya.
Baca juga: Jenis-Jenis dan Pembentukan Ikatan Kovalen
Contoh lainnya adalah antara molekul-molekul yang bersifat polar dimana terjadi dipol secara permanen. Hal ini menyebabkan senyawa polar dapat larut ke dalam pelarut polar. Sebagai contoh, asam asetat dapat larut di dalam air.
Terjadinya gaya ini yaitu sebagai berikut, mulaya dipol yang permanen tersebut mulai menginduksi lawan elektron molekul yang bersifat non polar. Akibatnya terbentuk dipol terinduksi. Adanya dipol terinduksi tersebut menyebabkan molekul yang bersifat non polar bisa larut ke dalam pelarut polar meskipun sedikit. Contoh, oksigen yang larut di dalam air.
Nah, apabila interaksi tarik-menarik atau tolak menolak terjadi pada ion (baik itu positif atau negatif) dengan molekul dipol permanen, maka dinamakan dengan gaya ion dipol.
3. Ikatan Hidrogen
Selanjutnya terdapat ikatan hidrogen. Ikatan ini merupakan gaya tarik menarik yang terjadi antara atom hidrogen di dalam senyawa-senyawa yang terdapat ikatan antara hidrogen dengan atom N, O, dan F. molekul polar seperi H2O mempunyai ujung-ujung yang muatannya saling berlawanan. Di dalam molekul, dipol menata dirinya sendiri sehingga sisi bermuatan positif akan berdekatan dengan sisi yang negatif.
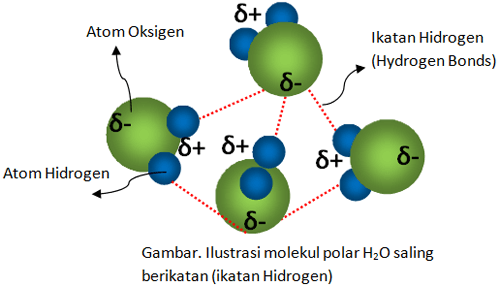
Kemudian tarikan dipol yang sangat kuat terjadi di antara molekul apabila memiliki atom hidrogen yang terikat dengan Nitrogen, Oksigen, atau Fluorin. Ujung positif dipol bisa mendekat ke arah ujung dipol negatif molekul lain, sehingga keduanya saling berdekatan dan terjadi gaya tarik menarik yang sangat kuat yang disebut dengan ikatan hidrogen. Kekuatan ikatan hidrogen mencapai 5-10% daripada ikatan kovalen.
Nah, bila ada pertanyaan terkait macam-macam gaya antar molekul beserta contohnya di atas. Bisa ditulis dalam kotak komentar di bawah ini
Referensi:
Brady, James E. 1994. Kimia Universitas Asas dan Struktur, terj. Edisi ke-5 Jilid 1. Jakarta: Erlangga.
Cotton and Wilkinson. 1989. Kimia Anorganik Dasar,terj. Jakarta: Penerbit Universitas Indonesia.