Apa itu pengertian ikatan kovalen ? apa saja jenis-jenis dan pembentukan ikatan kovalen itu ?. Nah, untuk menjawab pertanyaan ini kita akan bahas semuanya di halaman ini.
A. Pengertian ikatan Kovalen
Ikatan kovalen merupakan ikatan yang terjadi karena adanya pasangan elektron (e–) yang dipakai secara bersama-sama oleh atom-atom yang berikatan.
Adapun pasangan elektron yang dipakai bersama-sama dinamakan Pasangan Elektron Ikatan (PEI) sedangkan pasangan elektron yang tidak terlibat atau ikut dalam pembentukan ikatan kovalen, kita namakan sebagai Pasangan Elektron Bebas (PEB).
Ada lagi satu istilah yang harus dipahami yaitu senyawa kovalen. Apa itu? senyawa kovalen merupakan senyawa yang hanya mengandung ikatan kovalen saja. Nah, ikatan kovalen itu sendiri biasanya terjadi pada atom-atom unsur nonlogam baik itu sejenis maupun berbeda jenis.
Atom nonlogam sejenis misalnya O2, N2, Br2, F2, I2, Cl2 dan H2. Atom yang berbeda jenis nonlogamnya, misalnya H2O, CO2 dan sebagainya. Untuk mengetahui macam-macam atom nonlogam, bisa dibaca tentang memahami unsur-unsur dalam kimia atau jika temen-temen siswapedia ingin melihat tabel periodik unsur, bisa buka halaman ini: tabel periodik unsur.
Dalam menggambarkan ikatan kovalen ini kita dapat menggunakan rumus Lewis yaitu berupa sepasang titik o dan x yang menggambarkan pasangan elektron ikatan (PEI) atau bisa juga menggunakan satu garis (-). Sedangkan untuk pasangan elektron bebas (PEB) digambarkan sebagai dua buah titik oo.
Masih bingung? perhatikan contoh ikatan kovalen berikut ini.
a. H2

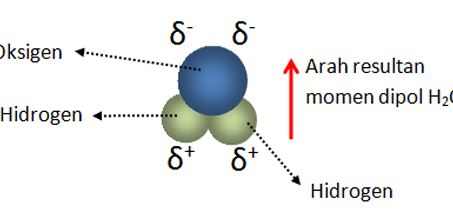
b. H2O

B. Jenis-jenis dan pembentukan ikatan kovalen
Apa saja macam-macam atau jenis-jenis ikatan kovalen itu?. Biar lebih paham, kita akan bahas pula contoh-contoh ikatan kovalen beserta proses pembentukan ikatan kovalen.
Macam-macam ikatan kovalen berdasarkan jumlah PEI dapat dibagi menjadi tiga yakni:
a. Ikatan kovalen tunggal
Ikatan kovalen tunggal merupakan ikatan kovalen yang memiliki 1 pasang PEI (Pasangan elektron Ikatan).
Contoh:
H2 dan H2O memiliki konfigurasi elektron H=1 dan O=2,6
H2 ditulis H – H
H2O ditulis H – O – H
b. Ikatan kovalen rangkap dua
Ikatan kovalen rangkap dua merupakan ikatan kovalen yang memiliki 2 pasang PEI (Pasangan elektron Ikatan).
Contoh:
O2, CO2 memiliki konfigurasi elektron O=2,6 dan C=2,4
Untuk mencapai kestabilan, maka atom O harus menerima 2 elektron. Nah, jika ada 2 atom O berdekatan, maka masing-masing akan saling memberi dan menerima dua atom sehingga O2 ditulis O = O
Untuk mencapai kestabilan, maka atom C (pada senyawa CO2) harus membutuhkan 4 elektron sedangkan atom O membutuhkan 2 elektron. Maka, atom C akan menggunakan bersama 2 elektron dari masing-masing atom O sedangkan pada masing-masing atom O akan menggunakan bersama 2 elektron dari atom C.
CO2 ditulis O = C = O
c. Ikatan kovalen rangkap tiga
Ikatan kovalen rangkap tiga merupakan ikatan kovalen yang memiliki 3 pasang PEI (Pasangan ikatan kovalen).
Contoh:
N2 memiliki konfigurasi elektron N=2,5
Untuk mencapai kestabilan, maka atom N harus menerima 3 elektron. Nah, jika ada 2 atom N berdekatan, maka masing-masing akan saling memberi dan menerima tiga atom sehingga menjadi N = N
Ikatan kovalen terjadi antara atom nonlogam yang satu dengan atom nonlogam lainya untuk mencapai kestabilan sesuai kaidah duplet atau oktet. Jika temen-temen bingung terkait kaidah duplet atau oktet, maka bacalah artikel berjudul Ikatan Kimia.
Lalu, pertanyaannya: apakah kaidah duplet dan oktet akan selalu berlaku?
Jawabannya adalah tidak. Coba perhatikan gambar struktur Lewis pada PCl3 dan PCl5 di bawah ini. (sumber gambar: Iman Rahayu dalam Praktis Belajar Kimia, hal.47)
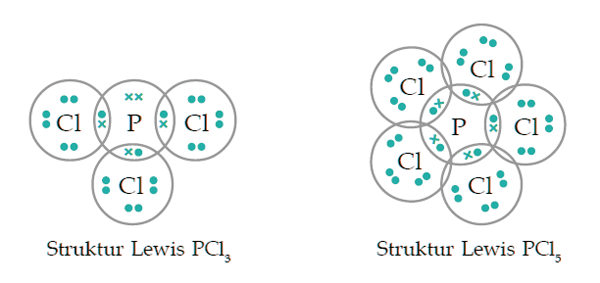
Atom P (Fosfor) memiliki 5 elektron terluar (valensi) sedangkan atom Cl (Klorin) memiliki 7 elektron terluar. Untuk mencapai kesetimbangan atom P membutuhkan 3 elektron sedangkan atom Cl membutuhkan 1 elektron lagi. Maka sesuai kaidah oktet, terbentuklah PCl3.
Namun, pada senyawa PCl5 hanya Cl sajalah yang memenuhi kaidah oktet sedangkan atom P tidak memenuhi karena memiliki elektron terluar berjumlah 10 elektron.
Contoh lainnya senyawa yang tidak memenuhi kaidah okted atau duplet adalah BF3.
Nah, terkait artikel jenis-jenis dan pembentukan ikatan kovalen di atas, apakah ada pertanyaan?. Untuk halaman selanjutnya kita akan membahas tentang macam-macam ikatan kovalen bedasarkan kepolaran ikatan yang diberi judul Ikatan Kovalen Nonpolar, Polar dan Koordinasi.