Hukum Perbandingan Volume oleh Gay Lussac – Dalam berbagai ilmu kita membutuhkan teori-teori dan hukum yang menjelaskan bagaimana sebuah ilmu bisa diterima. Salah satu contoh yaitu ilmu kimia. Ada beberapa macam hukum yang digunakan dalam kimia di mana hukum ini menjadi sumber lahirnya teori lain. Beberapa hukum kimia tersebut meliputi hukum perbandingan tetap, kelipatan perbandingan, kekekalan massa, dan perbandingan volume.
Dalam pembahasan kali ini akan lebih detal menjelaskan tentang hukup perbandingan volume yang ditemukan oleh ilmuwan bernama Gay Lussac. Hukum ini disebut juga dengan Hukum Gay Lussac, sesuai nama penemunya. Bagaimana sejarah Gay Lussac, penemuan, dan aplikasi Hukum Perbandingan Volume? Berikut penjelasan selengkapnya.
Baca juga: Hukum Kekekalan Massa
Sejarah Joseph Louis Gay Lussac
Seorang ahli di bidang kimia dan fisika bernama Joseph Louis Gay Lussac ini telah berjasa dalam bidang kimia. Ia telah menemukan suatu teori yang mendasari perkembangan teori kimia yang lain yaitu Hukum Perbandingan Volume. Selain itu ia juga dikenal sebagai ilmuan yang berkaitan dengan gas.
Gay Lussac dilahirkan di Vienne tepatnya tanggal 6 Desember 1778. Di tahun 1802, Gay Lussac pertama kali mencetuskan sebuah hukum kimia yang merupakan hasil dari percobaannya. Dalam rumusannya, ia mengatakan bahwa massa dan volume suatu gas yang dipertahan agar tetap konstan akan berpengaruh pada tekanan gas.
Tekanan gas ini akan meningkat seiring dengan meningkatnya temperatur. Hukum ini pun dikenal dengan P = k T (P untuk tekanan, k untuk tetapan gas, dan T untuk suhu dalam satuan Kelvin). Rumus ini juga bisa dipahami sebagai P/T = k. Kemudian dari rumus tersebut kita mengenal bahwa tekanan akan berbanding lurus dengan suhu.
Baca juga : Hukum-hukum dasar dalam ilmu kimia
Hukum ini bisa benar karena temperatur atau suhu diukur dari rerata suatu energi kinetik dari zat. Energi kinetik tersebut akan meningkat apabila partikel-partikel bertumbukkan dengan pergerakan yang cepat. Hal ini akan berpengaruh pada peningkatan tekanan.
Penemuan Hukum Perbandingan Volume
Untuk dapat merumuskan sebuah teori atau hukum di ilmu pengetahuan seperti kimia, maka diperlukan serangkaian penelitian yang mampu menjelaskan teori tersebut nantinya. Gay Lussac tidak menemukannya dalam satu kali penelitian namun berbagai reaksi telah ia coba.
Ia menemukan bahwa untuk setiap satu satuan volume suatu gas hidrogen ternyata bereaksi dengan 1 satuan volume gas Cl2 atau gas klorin. Reksi ini akan menghasilkan 2 satuan volume gas HCl (hidrogen klorida). Sehingga perbandingan volume yang didapatkan yaitu 1:1:2 untuk volume gas hidrogen, klorin, dan hidrogen klorida secara berturut-turut.
Oleh karena itu, Gay Lussac akhirnya berhasil merumuskan sebuah hukum kimia yaitu sebagai berikut.
“volume beberapa gas yang bereaksi dan volume gas hasil reaksi tersebut apabila diukur di suhu dan tekanan yang sama, maka akan berbanding menghasilkan bilangan bulat dan sederhana.”
Hukum ini kemudian menjadi sebuah landasan yang penting bagi stoikiometri gas modern. Selain itu Hukum Gay Lussac menjadi dasar lahirnya hukum Avogadro yang juga membahas tentang suhu dan tekanan pada suatu molekul.
Aplikasi Hukum Perbandingan Volume Oleh Gay Lussac
Untuk lebih memahami hukum perbandingan volume, simak contoh penggunaannya di bawah ini.
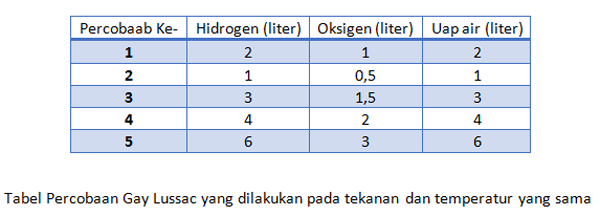
Apabila anda mereaksikan 2 satuan volume gas hidrogen dengan 1 satuan gas oksigen, maka reaksi ini akan menghasilkan 1 satuan volume uap air (H2O). dari hasil ini maka akan diperoleh sebuah perbandingan gas hidrogen, oksigen, dan uap air yaitu 2:1:2 yang merupakan bilangan bulat dan sederhana.
Sumber :
Brady, James E. 1990. General Chemistry, (Principles & Structures). New York: John Wiley and Sons.
Chang, R. 2005. Chemistry. 8th ed. New York: Mc-Graw Hill.
Keenan, Charles E. et. al, – Pudjaatmaka. 1999. Ilmu Kimia Universitas (terjemahan). Jakarta: Erlangga.