Reaksi Reduksi dan Oksidasi (Redoks) sering kita temukan dalam kehidupan sehari-hari misalnya pada reaksi pembakaran, pembuatan larutan cuka, reaksi metabolisme di dalam tubuh, dan lain sebagainya.
Reaksi reduksi dan oksidasi mengalami perkembangan sehingga mampu menjelaskan proses perubahan kimia dalam berbagai peristiwa.
Perkembangan Kosep Reaksi Redoks
Pada mulanya reaksi oksidasi diartikan sebagai reaksi pengikatan oksigen oleh zat tertentu. Sedangkan reaksi reduksi adalah reaksi pelepasan oksigen. Contoh reaksinya yaitu:
Oksidasi : H2(g) + ½ O2 (g) → H2 (l)
Reduksi : FeO (s) + CO (g) → Fe (s) CO2 (g)
Namun pendapat tersebut dinilai kurang menjelaskan reaksi kimia secara luas karena banyak reaksi yang tidak melibatkan oksigen. Kemudian konsep redoks berkembang dimana reaksi oksidasi merupakan reaksi yang melibatkan pelepasan elektron dan reaksi reduksi adalah reaksi yang melibatkan pengikatan elektron.
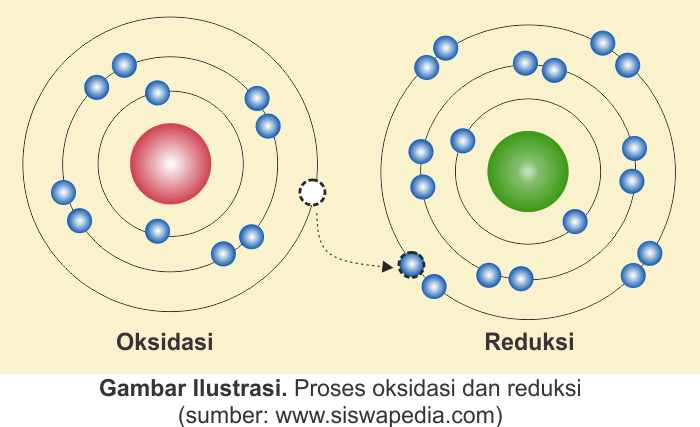
Konsep tersebut ditunjukkan oleh persamaan reaksi kimia berikut.
Na(s) + ½ Cl2 (g) → NaCl (s)
Reaksi di atas melibatkan dua peristiwa:
Oksidasi : Na (s) → Na+ (s) + e-
Reduksi : ½ Cl2 (g) + e- → Cl- (s)
Konsep ini menjelaskan bahwa pengikatan dan pelepasan elektron terjadi secara bersamaan. Transfer elektron terjadi pada senyawa yang beriktan ion. Itu berarti konsep ini hanya dapat menjelaskan reaksi yang melibatkan senyawa-senyawa ion tetapi tidak dapat menjelaskan reaksi yang melibatkan senyawa kovalen.
Artikel terkait: Metode lumpur aktif sebagai aplikasi redoks
Konsep redoks berkembang yang menghasilkan teori bahwa terdapat suatu bilangan yang disebut dengan bilangan oksidasi.
Bilangan Oksidasi dalam Konsep Redoks
Bilangan oksidasi adalah suatu bilangan bulat yang menyatakan tingkat oksidasi suatu unsur yang membentuk senyawa. Bilangan oksidasi atau biloks dapat ditentukan berdasarkan ikatan dan struktur suatu zat. Bilangan tersebut merupakan muataan riil suatu ion dalam suatu senyawa.
Pada senyawa kovalen, bilangan oksidasi ini merupakan skala tingkat keelektronegatifan masing-masing atom penyusun senyawa itu sendiri. Semakin tinggi elektronegatifan atom maka semakin kuat daya tariknya terhadap pasangan elektron sehinga bernilai negatif.
Namun sebaliknya jika keelektronegatifitas suatu atom lebih rendah maka nilainya semakin positif.
Adapun aturan penentuan bilangan oksidasi adalah sebagai berikut.
- Atom di golongan IA seperti Li, Na, K, Rb, Cs, serta Fr selalu mempunyai biloks +1
- Pada golongan IIA seperti Be, Mg, Ca, Sr, dan Ba, selalu memunyai biloks +2
- Untuk golongan IIIA seperti atom B, Al, serta Ga selalu memiliki biloks +3.
- Atom hidrogen atau H umumnya didalam senyawa memiliki bioloks +1, kecuali untuk senyawa-senyawa hidrida logam.
- Senyawa hidrida logam seperti LiH, CaH2, NaH, dan seterusnya atom hidrogen memiliki biloks -1.
- Umumnya atom oksigen atau O memiliki biloks -2, kecuali dalam senyawa-senyawa peroksida seperti H2O2, Na2O2, dan lain sebagainya.
- Pada senyawa peroksida tersebut atom O memiliki bilangan oksidasi bernilai +2.
Berikut Contoh Reaksi Redoks berdasarkan Bilangan Oksidasi
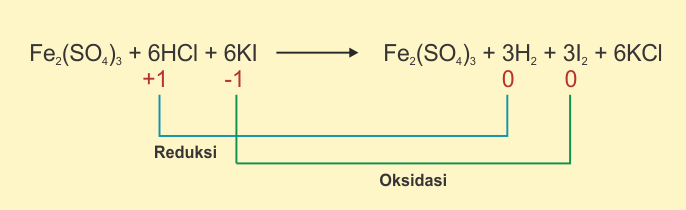
Perlu diingat bahwa reaksi oksidasi adalah reasi yang melibatkan kenaikan bilangan oksidasi. Sedangkan reaksi reduksi adalah reaksi yang diliputi oleh penurunan bilangan oksidasi. Berikut beberapa contohnya.
Baca juga: Contoh soal hukum Faraday 1 dan 2
Pengoksidasi dan Pereduksi
Didalam reaksi redoks atau reaksi reduksi oksidasi, terdapat agen pereduksi dan agen pengoksidasi. Pereduksi disebut juga reduktor, merupakan zat yang terlibat di dalam reaksi redoks yang menyebabkan zat lain mengalami reduksi. Sedangkan pengoksidasi atau oksidator yang terdapat di dalam reaksi redoks akan membuat zat lain mengalami oksidasi.
Dengan kata lain, zat reduktor akan mengalami oksidasi. Sedangkan zat oksidator akan mengalami reduksi. Pada contoh reaksi di bawah ini,
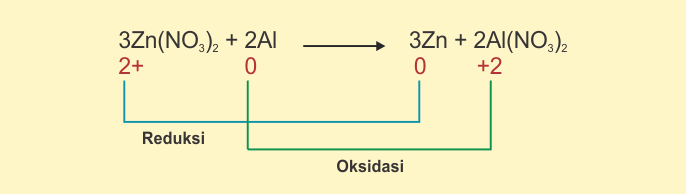
Zn(NO3)2 bertindak sebagai oksidator, maka senyawa ini mengalami reduksi. Sedangkan Al bertindak sebagai reduktor sehingga mengalami oksidasi.


